
Welke regeneratieve behandelingen zijn beschikbaar?
Regeneratieve geneeskunde is erop gericht nieuwe behandelingen te ontwikkelen die cellen, weefsels en orgaanfuncties repareren, vervangen of herstellen na schade door ziekte of letsel.
De behandelingen die op dit moment (januari 2022) zijn goedgekeurd in Europa en/of Nederland zijn:
Meer over toepassingen en behandelingen:
 Welke regeneratieve behandelingen zijn er beschikbaar voor knieartrose? Artrose in de knie is een groeiend probleem in onze samenleving dat in sommige gevallen kan worden behandeld met een regeneratieve behandeling met stamcellen.
Welke regeneratieve behandelingen zijn er beschikbaar voor knieartrose? Artrose in de knie is een groeiend probleem in onze samenleving dat in sommige gevallen kan worden behandeld met een regeneratieve behandeling met stamcellen.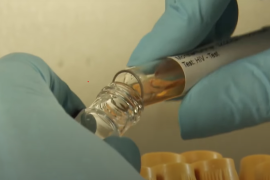 Kunnen stamcellen worden gebruikt bij de genezing van hiv? Een handjevol mensen is ooit genezen van hiv door een stamceltransplantatie. Maar hoe werkt zo’n behandeling en waarom wordt die nog niet bij iedereen toegepast?
Kunnen stamcellen worden gebruikt bij de genezing van hiv? Een handjevol mensen is ooit genezen van hiv door een stamceltransplantatie. Maar hoe werkt zo’n behandeling en waarom wordt die nog niet bij iedereen toegepast?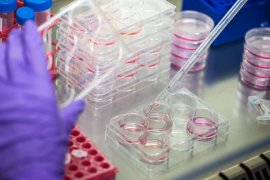 Kan RM leverschade behandelen of herstellen? Binnen de regeneratieve geneeskunde wordt onderzocht hoe stamcellen, gentherapie en bioprinten kunnen helpen wanneer de lever ernstig beschadigd is.
Kan RM leverschade behandelen of herstellen? Binnen de regeneratieve geneeskunde wordt onderzocht hoe stamcellen, gentherapie en bioprinten kunnen helpen wanneer de lever ernstig beschadigd is. Kan regeneratieve geneeskunde erfelijke stofwisselingsziekten genezen? Stofwisselingsziekten (metabole ziekten) zijn ernstig en moeilijk te behandelen. Met gentherapie wordt geprobeerd betere behandelingen te ontwikkelen.
Kan regeneratieve geneeskunde erfelijke stofwisselingsziekten genezen? Stofwisselingsziekten (metabole ziekten) zijn ernstig en moeilijk te behandelen. Met gentherapie wordt geprobeerd betere behandelingen te ontwikkelen. Kunnen stamcellen in de nabije toekomst toegepast worden voor herstel van het hart? Hart- en vaatziekten zijn wereldwijd de belangrijkste doodsoorzaak. Hoe wordt stamcelonderzoek ingezet voor het herstel van het hart?
Kunnen stamcellen in de nabije toekomst toegepast worden voor herstel van het hart? Hart- en vaatziekten zijn wereldwijd de belangrijkste doodsoorzaak. Hoe wordt stamcelonderzoek ingezet voor het herstel van het hart?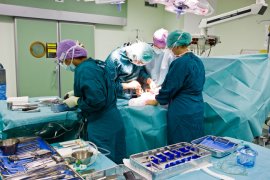 Welke regeneratieve behandelingen zijn beschikbaar? Een overzicht van de behandelingen die op januari 2022 zijn goedgekeurd in Europa en/of Nederland.
Welke regeneratieve behandelingen zijn beschikbaar? Een overzicht van de behandelingen die op januari 2022 zijn goedgekeurd in Europa en/of Nederland.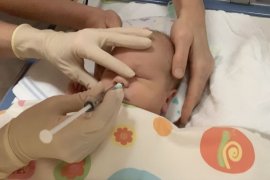 Kunnen stamcellen hersenschade herstellen? Baby’s met een herseninfarct kunnen veilig behandeld worden met stamcel-neusdruppels.
Kunnen stamcellen hersenschade herstellen? Baby’s met een herseninfarct kunnen veilig behandeld worden met stamcel-neusdruppels. Worden organoïden al gebruikt voor medicatie/therapiekeuze bij kankerpatiënten? Kanker is een complexe ziekte en de huidige behandelingen zijn vaak niet specifiek genoeg. Tumororganoïden kunnen helpen tot een behandeling op maat te komen.
Worden organoïden al gebruikt voor medicatie/therapiekeuze bij kankerpatiënten? Kanker is een complexe ziekte en de huidige behandelingen zijn vaak niet specifiek genoeg. Tumororganoïden kunnen helpen tot een behandeling op maat te komen. Is een regeneratieve behandeling veilig? Een behandeling wordt uitgebreid beoordeeld voordat het wordt goedgekeurd.
Is een regeneratieve behandeling veilig? Een behandeling wordt uitgebreid beoordeeld voordat het wordt goedgekeurd. Waar kan ik een regeneratieve behandeling krijgen? In Nederland zijn het vooral de academische ziekenhuizen. Neem contact op met je behandelend arts voor jouw specifieke situatie.
Waar kan ik een regeneratieve behandeling krijgen? In Nederland zijn het vooral de academische ziekenhuizen. Neem contact op met je behandelend arts voor jouw specifieke situatie. Navelstrengbloed bewaren, doen of niet? Aanstaande ouders kunnen navelstrengbloed van hun kind opslaan in een bloedbank. Om te doneren is dat zinvol, terwijl opslaan voor eigen gebruik dat niet is.
Navelstrengbloed bewaren, doen of niet? Aanstaande ouders kunnen navelstrengbloed van hun kind opslaan in een bloedbank. Om te doneren is dat zinvol, terwijl opslaan voor eigen gebruik dat niet is. Wat is stamceltoerisme en wat zijn de risico’s? In het buitenland bieden klinieken (onbewezen) stamcelbehandelingen aan die niet vergoed worden. Wat is stamceltoerisme en wat zijn de risico’s?
Wat is stamceltoerisme en wat zijn de risico’s? In het buitenland bieden klinieken (onbewezen) stamcelbehandelingen aan die niet vergoed worden. Wat is stamceltoerisme en wat zijn de risico’s? Kun je met stamcellen hele organen vervangen als deze niet meer werken? Onderzoekers bestuderen hoe je van stamcellen hele organen kunt maken. Dan kun je in de toekomst zieke organen vervangen of orgaantransplantatie overbodig maken.
Kun je met stamcellen hele organen vervangen als deze niet meer werken? Onderzoekers bestuderen hoe je van stamcellen hele organen kunt maken. Dan kun je in de toekomst zieke organen vervangen of orgaantransplantatie overbodig maken. Kan regeneratieve geneeskunde helpen bij verminderde nierfunctie? Onderzoekers werken hard aan technieken die dialyse effectiever, veiliger en minder ingrijpend kunnen maken.
Kan regeneratieve geneeskunde helpen bij verminderde nierfunctie? Onderzoekers werken hard aan technieken die dialyse effectiever, veiliger en minder ingrijpend kunnen maken. Kan regeneratieve geneeskunde echt genezen? Bij een regeneratieve behandeling wordt het lichaam aangezet om de ziekte zelf te herstellen.
Kan regeneratieve geneeskunde echt genezen? Bij een regeneratieve behandeling wordt het lichaam aangezet om de ziekte zelf te herstellen.



